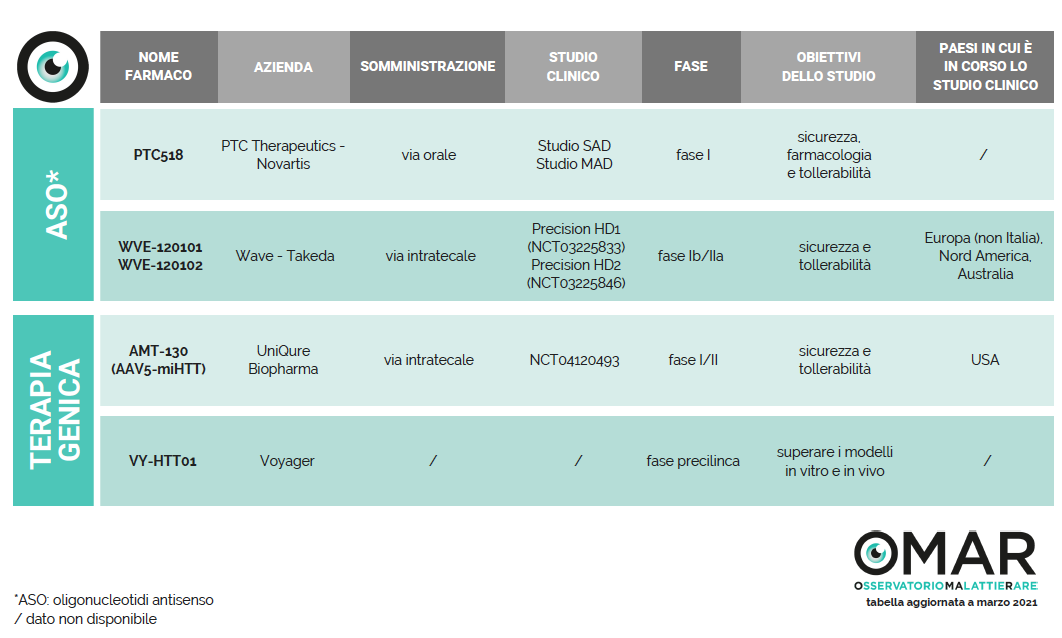
Oligonucleotidi antisenso (ASO) ma anche terapia genica e altre molecole attualmente in fase di studio, alcune delle quali per somministrazione orale. Ne parla la dott.ssa Caterina Mariotti (Milano).
Il panorama degli studi clinici per la malattia di Huntington basati sulla somministrazione di oligonucleotidi antisenso (ASO) e sulla terapia genica ha subito nelle ultime settimane alcuni cambiamenti importanti caratterizzati da un lato dalla brusca interruzione del trial di Roche con il farmaco tominersen e, dall’altro, dalla buona notizia della conclusione della prima parte dello studio UniQure con AMT-130.
La ricerca si sta concentrando sulla possibilità di arrestare la progressione della malattia di Huntington, attraverso il ricorso a molecole che degradino l’mRNA che codifica per l’huntingtina mutata sfruttando il meccanismo d’azione degli ASO, o utilizzando la terapia genica. Su entrambi questi fronti stanno giungendo notizie interessanti, oltre a novità relative a molecole di più facile somministrazione (in particolar modo per via orale).
GLI ASO DI WAVE LIFE SCIENCES
Wave Life Sciences è una biotech da tempo impegnata nel campo degli oligonucleotidi antisenso che ha sviluppato una molecola ad azione selettiva in grado di agire sulla forma mutata della huntingtina. Il farmaco, o meglio i farmaci (WVE-120101 e WVE-120102) sono prodotti da Takeda e, fino a poco tempo fa, erano in fase di studio in due trial clinici multicentrici, randomizzati, in doppio cieco, controllati con placebo, di Fase Ib/IIa, denominati rispettivamente PRECISION-HD1 e PRECISION-HD2. Purtroppo, a poca distanza dalla notizia dell’interruzione del trial clinico di Roche, anche Wave Life Sciences ha comunicato l’interruzionel’interruzione dei programmi di ricerca PRECISION-HD1 e -HD2. Una prima analisi dei dati provenienti da entrami gli studi clinici ha messo in evidenza che il trattamento non ha raggiunto lo scopo principale in quanto non ha prodotto una riduzione significativa nei livelli di huntingtina mutata nei pazienti che hanno ricevuto il farmaco rispetto a quelli che hanno ricevuto il placebo. Non sono stati evidenziati cambiamenti in nessuno dei diversi dosaggi testati. Ciò significa che i farmaci non hanno esercitato l’effetto sperato: in particolare, per quanto riguarda la molecola nota come WVE-120102 si è visto che i risultati in tutti gli 88 partecipanti al trial PRECISION-HD2 non hanno dimostrato alcun cambiamento significativo nei livelli di huntingtina. In maniera analoga è naufragato anche lo studio PRECISION-HD1 dedicato a WVE-120101.
“Nei trial clinici di Wave Life Sciences erano in valutazione la sicurezza e la tollerabilità delle due molecole che, sfruttando un approccio allele-selettivo, puntavano al silenziamento esclusivo del pre-mRNA dell’allele mutato mantenendo attivo quello sano”, spiega la dott.ssa Caterina Mariotti, dell’U.O.C. di Genetica delle Malattie Neurodegenerative e Metaboliche presso l’Istituto Neurologico Carlo Besta di Milano. “Queste molecole prendevano di mira due polimorfismi che, qualora presenti, avrebbero permesso di individuare l’mRNA della proteina mutata senza interferire con quello della proteina sana”. Infatti, la forma sana di huntingtina migliora la risposta allo stress ossidativo, favorisce la circolazione di nutrienti essenziali e regola la comunicazione tra neuroni, contribuendo a mantenere in buona salute le cellule del cervello. Come per l’ASO di Roche, anche in questo caso la somministrazione è avvenuta per via intratecale. Diversamente dal farmaco prodotto dalla multinazionale svizzera, per le sperimentazioni di Wave non c’erano centri italiani coinvolti nei due studi, che sono stati condotti in altri paesi Europei, in Nord-America e Australia.
Wave Life Science ha tuttavia annunciato che non rinuncerà all’impegno contro la malattia di Huntington, puntando su una terza molecola, WVE-003, che sarà testata in uno studio clinico di Fase Ib/IIa. Si tratta di una molecola diversa, ideata per aumentare l’affinità per l’mRNA. È considerata una speranza per il futuro insieme all’altra terapia genica - denominata VY-HTT01 e sviluppata da Vojager Therapeutics - che ancora è in fase pre-clinica.
LA PRIDOPIDINA DI PRILENIA
Sul versante delle molecole farmacologiche a somministrazione orale vale la pena menzionare uno studio che coinvolgerà un grande numero di pazienti, anche Italiani. Si tratta del farmaco
Pridopidina, e lo studio è denominato PROOF-HD. “Pridopidina è un farmaco che ha rivelato un buon profilo di sicurezza in diversi studi condotti precedentemente”, continua Mariotti. “Nello specifico la Pridopidina è un agonista altamente selettivo del recettore Sigma-1 (S1R), una proteina del reticolo endoplasmatico che partecipa a diversi processi cellulari”, spiega Mariotti. Attualmente è in corso uno studio clinico multicentrico randomizzato, in doppio cieco, controllato con placebo, di Fase III. “Ad oggi, lo studio risulta attivo negli Stati Uniti, in Canada e in diversi paesi Europei tra cui l’Italia”.
Da studi precedenti i ricercatori hanno notato una possibile efficacia del farmaco nel rallentare la malattia particolarmente in pazienti che si trovano negli stadi iniziali (stadio I e II), favorendo quindi una stabilizzazione iniziale del quadro clinico.
“I ricercatori intendono valutare l’effetto della molecola sulle funzioni motorie e comportamentali dei pazienti analizzando i punteggi delle scale motorie e funzionali, quali la Unified Huntington Disease Rating Scale-Total Tunctional Capacity (UHDRS-TFC) score, e confrontando i risultati ottenuti dai pazienti prima e dopo la somministrazione del farmaco”, precisa ancora.
ALTRI FARMACI ALLO STUDIO
Ulteriori molecole in studio comprendono il farmaco ANX005, un anticorpo monoclonale da somministrare in vena, sviluppato da Annexion e attualmente in Fase II e VX15, un anticorpo monoclonale sviluppato da Vaccinex e diretto contro la semaforina4D (SEMA4D) che si somministra in vena e interferisce con la progressione dei processi neuro-infiammatori. Per quest’ultimo lo studio clinico di riferimento è SIGNAL di Fase II. In aggiunta a questi è in fase di valutazione anche la valbenazina, un inibitore del trasportatore vescicolare delle monoamine di tipo II (VMAT2), sul quale risulta in corso lo studio clinico KINECT HD, di Fase III promosso da Neurocrine Biosciences e Huntington Study Group i cui risultati sono attesi per la prima metà del 2021. “Infine, un’ultima molecola che merita attenzione e sembra agire riducendo i livelli di huntingtina è Branaplam (LMI070), prodotto da Novartis”, conclude Mariotti. “Si tratta di un farmaco in sperimentazione contro la SMA ma che Novartis conta di testare anche su pazienti affetti da malattia di Huntington con avviare uno studio clinico di Fase II-b che dovrebbe essere avviato entro il 2021”. Una prospettiva decisamente incoraggiante per una malattia come la Huntington che ancora manca di una terapia specifica.